Ю. В. Булавкин, А. Н. Лавров, С. А. Столярова
Донозологическая оценка иммунологического статуса детей, проживающих в зоне экологического риска
Известно, что на здоровье детей оказывают негативное влияния неблагоприятные факторы внешней среды. Их воздействие усугубляется при снижении уровня профилактической работы и это приводит к росту заболеваемости населения, особенно детей и подростков [1]. На многих территориях планеты, в том числе и России, имеются районы, населенные пункты, характеризующиеся неблагоприятной экологической обстановкой [2]. В связи с этим и проводимой в стране диспансеризацией детского населения, направленной на прогнозирование здоровья подростков, важна оценка состояния иммунной системы у детей.
Целью работы явилось донозологическая оценка иммунного статуса у детей Пензенского района Пензенской области, проживающих в зоне предполагаемого экологического риска.
Пациенты и методы
В исследование включили 169 детей в возрасте от 8 до 16 лет, проживающих и обучающихся в школах 3 населенных пунктов Пензенского района Пензенской области, условно обозначенные А, В, С. В зависимости от места проживания и удаленности от мест хранения и уничтожения химического оружия все дети были выделены в три сравнимые группы по возрасту и полу. Названия группы получили соответственно названию населенных пунктов: А, В, С. Населенные пункты перечислены в порядке удаления от мест уничтожения химоружия. Наиболее дальний – населенный пункт «A», его дети были отнесены в контрольную группу. Дети более близких населенных пунктов «В» и «С» составили группы сравнения. При изучении показателей в зависимости от пола детей трех групп делили на 2 подгруппы: девочек (всего 88 детей, средний возраст 11,5 лет) и подгруппу мальчиков (всего 81 ребенок, средний возраст 12,5 лет).
Обследование детей проводили согласно протоколу ВОЗ [3]. Антропометрические исследования включали измерение роста и массы тела. Психометрию по таблицам Шульте–Горбова [4]. Кровь для биохимических исследований забиралась утром натощак. Гуморальный иммунитет оценивали по уровню трех классов иммуноглобулинов IgG, IgA, IgM.
Для диагностики аутоагрессии против нормальных компонентов организма использовали определение уровня специфических антител к отдельным органам и тканям.
Иммунный статус щитовидной железы оценивали по специфическим аутоантителам к тиреоглобулину (анти-ТГ) и аутоантителам к тиреопероксидазе (антиТПО). Иммуноглобулины определяли иммунотурбодиметрическим методом, пользуясь наборами реактивов фирмы «Диакон-Diasys» (Германия). Количество аутоантител к тиреоглобулину и тиреопероксидазе щитовидной железы оценивали методом ИФА. Для определения антител анти-ТГ IgG и анти-ТПО IgG использовали тест-системы фирмы «Labodia S.A.,Yens». Статистическую обработку осуществляли с помощью компьютерной программы Microsoft Exell 5.1.
Результаты исследования и их обсуждение
Одним из объективных критериев роли иммунной системы в устранении потенциально вредных для гомеостаза экзо- и эндогенных (аутоиммунных) токсических метаболитов, отклонений в гомеостазе являются изменения в сыворотке крови основных классов иммуноглобулинов IgG, IgA, IgM и уровень аутоантител [5–7]. В табл. 1 представлена сравнительная характеристика гуморального иммунитета по основным классам иммуноглобулинов IgG, IgA, IgM и клеточного (органного), характеризующего нарушение функции щитовидной железы анти-ТГ и анти-ТПО у детей в зависимости от степени экологического риска и пола. Из таблицы видно, что абсолютно у всех детей, проживающих в населенных пунктах А, В, С, средние величины (M ± m) колебались в пределах верхних и нижних референсных значений нормы. Однако отмечено, что по мере приближения к местам уничтожения химического оружия происходило снижение IgA (M ± m) к нижним границам норм, и, наоборот, по мере удаления их значения смещались к верхним границам нормы.
Необходимо указать на неоднозначность колебаний полученных средних величин иммуноглобулинов.
у детей (девочек и мальчиков), проживающих в зоне экологического риска
| Показатели | Пензенский район | |||||
| Контрольная группа | Вторая группа | Третья группа | ||||
| Девочки
(n = 18) |
Мальчики
(n = 8) |
Девочки
(n = 30) |
Мальчики
(n = 31) |
Девочки
(n = 41) |
Мальчики
(n = 41) |
|
| IgA, г/л | 2,3 ± 0,22 | 1,93 ± 0,1 | 1,87 ± 0,022** | 1,69 ± 0,1* | 1,37 ± 0,12* | 1,17 ± 0,1* |
| IgG, г/л | 12,43 ± 1,04 | 13,13 ± 0,8 | 12,78 ± 0,21 | 12,27 ± 0,68 | 12,44 ± 1,0 | 12,02 ± 0,68 |
| IgM, г/л | 2,26 ± 0,21 | 1,59 ± 0,2 | 1,78 ± 0,21** | 1,99 ± 0,2** | 2,2 ± 0,21 | 2,26 ± 0,2** |
| анти-ТГ МЕ/мл |
11,69 ± 1,43 | 16,37 ± 2,78 | 68,39 ± 3,5** | 58,88 ± 3,8* | 48,01 ± 2,0** | 34,38 ± 1,6* |
| анти-ТПО МЕ/мл |
9,94 ± 1,16 | 12,63 1,93 | 24,05 ± 2,0** | 30,21 ± 2,2* | 64,2 ± 0,9*** | 17,92 ± 0,6 |
Примечание: n – число обследованных; р – достоверность различий по отношению к контролю;
* < 0,05; **< 0,01; ***< 0,001.
Содержание иммуноглобулинов класса IgG в сыворотке крови у девочек контрольной группы (А, наиболее удаленный населенный пункт) соответствовало средним значениям IgG девочек групп «В» и «С». У мальчиков групп «В» и «С» при сравнении с результатами контрольной группы, так же достоверных колебаний иммуноглобулина класса IgG в сыворотке крови не выявлено (см. табл.1).
Иммуноглобулины класса IgM являются самыми крупными антителами в сыворотке крови. Это единственный класс антител, синтез которых начинается еще до рождения ребенка. И IgM способны нейтрализовать инородные частицы и эффективно активировать систему комплемента, запустить ответную реакцию организма [8].
При сравнении результатов исследования иммуноглобулинов класса IgМ в сыворотке крови детей групп «В» и «С» с их величиной контрольной группы были получены неоднозначные значения. Достоверно увеличивалось количество IgМ у мальчиков В (p < 0,01) и С (p < 0,01) групп обследуемых детей и снижалось у девочек «В» группы (p < 0,01) (рис. 1).
Иммуноглобулины класса IgA составляют 10–15% иммуноглобулинов сыворотки. Наиболее важная форма IgA – это секреторные IgA. Секреторные IgA осуществляют местную защитную реакцию против бактериальных и вирусных антигенов, контактирующих со слизистыми оболочками. Секреторные IgA, продуцируются В-клетками, внутри слизистого слоя селективно связываются с бактериями и предупреждают их адгезию к стенке [9].
Анализ содержания в крови иммуноглобулинов класса IgА, выявил, что по мере приближения к местам уничтожения химического оружия независимо от половой принадлежности происходило их снижение (М ± m) к нижним границам нормы. Наиболее значимыми изменения оказались у детей, проживающих в группе «С» (p < 0,01). Снижение IgA у девочек в 1,67 (p < 0,01), у мальчиков в 1,65 раза (p < 0,01) относительно содержания IgА детей контрольной группы (см. табл. 1). Таким образом, установили изменения в иммунном статусе за счет снижения в сыворотке крови иммуноглобулинов класса IgA в ближайшем («С») и промежуточном («В») населенном пунктах к местам уничтожения химоружия.
Наиболее важными критериями доклинических нарушений от экзогенной и эндогенной интоксикации, на наш взгляд, являются рост в сыворотке крови специализированных тканевых антител к тиреоглобулину (анти-ТГ), тиреоидной пироксидазе (анти-ТПО) и рецепторам к тиреотропному гормону [8, 9]. Разрушение специализированных клеток (тироцитов) под действием экзогенных и эндогенных факторов ведет к поступлению в кровь аутоантигенов (аутоАГ) и по принципу обратной связи сопровождается ростом аутоантител [10]. По литературным данным рост антител бывает раньше, чем появляются клинические признаки основного заболевания [11, 12].
Сравнивая результаты исследования специфических антител к тиреоглобулину (анти-ТГ IgG) в сыворотке крови девочек «В» и «С» групп с контрольной группой детей «А», установили значительное повышение показателя анти-ТГ IgG в С в 4,1 (p< 0,01) раза и «В» – в 5,8 (p < 0,01) раза. У мальчиков группы «С» анти-ТГ был выше в 2,1 (p < 0,01) раза, в группе «В» – в 3,59 (p < 0,01) раза (см. табл. 1).
Уровень аутоантител анти-ТПО у девочек был выше в группе «С» в 6,4 (p < 0,01) раза, в группе «В» в 2,4 (p < 0,01) относительно девочек контрольной группы. У мальчиков группы «С» величина анти-ТПО была выше в 1,4 (p < 0,01) раза, в группе «В» выше в 2,39 (p < 0,01) раза, чем у мальчиков контрольной группы.
Из данных табл. 1 и рис. 1 видно, что по мере удаления от места хранения и уничтожения химического оружия изменений количество анти-ТГ IgG и анти-ТПО IgG было меньше как у мальчиков, так и у обследованных девочек.
Если рассмотреть полученные данные по всем населенным пунктам «А», «В», «С» (см. табл. 1), то отклонения от нормы в количестве аутоантител к тиреопероксидазе (анти-ТПО IgG) и тиреоглобулину анти-ТГ IgG были в контрольной группе только у одной девочки из 18 (6 ± 6%). Антитела к тиреопироксидазе (анти-ТПО IgG) в группе «В» были выше нормы у одной девочки из 30 (3 ± 3) и у 4 мальчиков из 31 (12 ± 6 %). В группе «С» анти-ТГ IgG повышен был у трех девочек (8 ± 4), анти-ТПО IgG увеличен у 6 (15 ± 5 %, у 5-и девочек и у 1-го мальчика).
В генезе аутоиммунности остается много нерешенных вопросов [13–15], главный из которых сводится к следующему: где локализуется первичный дефект? Иными словами, является ли орган, против которого направлена иммунная атака, исходно интактным, или в нем возникают какие-то первичные нарушения, которые придают его клеткам свойства «чужеродных» и вызывают нормальную реакцию иммунной системы [16].
Описаны нарушения при аутоиммунных заболеваниях щитовидной железы в системе молекулярной регуляции межклеточных взаимодействий. Для АИТ свойственны нарушения передачи сигналов регуляторными субстанциями за счет блокирования их эндоцитоза, а при диффузном токсическом зобе уровень эндоцитоза не снижается, но отмечается выраженный дисбаланс биосинтеза ТТГ, α−ФНО, ИЛ−6, макроглобулинов. Определение ауто-АТ позволяют выявить маркерные изменения в организме обследуемого задолго до клинической манифестации патологии [5].
Пластичность адаптивных и компенсаторных реакций у детей способна пролонгировать латентный период развития тиреоидной патологии и сместить ее выявление на более поздний возраст [17].
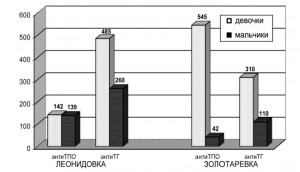
Рис. 1. Сравнительная оценка колебаний уровней специфических антител анти-ТГ и анти-ТПО у детей групп «В» и «С»
Таким образом, у обследованных детей групп «В» и «С», проживающих в зоне экологического риска, обнаружены диагностические титры аутоантител анти-ТГ IgG и анти-ТПО IgG, превышающие величину показателей в контрольной группе. Это свидетельствует об активации адаптационно-приспособительных механизмов и развитием дисфункции щитовидной железы. Количество аутоантител анти-ТПО IgG у детей группы «В» при сравнении с результатами контрольной было повышено и у девочек, и у мальчиков. Необходимо отметить, что у детей группы «С» более высокие
титры анти-ТПО IgG были выявлены у девочек. Количество аутоантител анти-ТГ IgG в «В» и «С» группах менялись однонаправлено относительно показателя детей контрольной группы. Подобные отклонения в иммунном статусе характеризуются рассогласованием в функциях и взаимосвязях различных звеньев антигенно-структурного гомеостаза на уровне щитовидной железы, особенно в группе девочек.
Сравнительная оценка результатов исследования иммунного статуса детей групп «В» и «С» относительно контрольной группы показало подавление выработки иммуноглобулинов класса IgA и увеличение количества иммуноглобулинов IgМ, а также повышение количество аутоантител анти-ТПО преимущественно у девочек групп «В» и «С», а аутоантитела анти-ТГ и анти-ТПО – у детей группы «С». Увеличение количества иммуноглобулинов IgМ подтверждает развитие аутоиммунного процесса в самой щитовидной железе [18].
Выводы
1. Установлены особенности изменения в иммунологическом статусе у детей населенных пунктов в зависимости от удаления от мест уничтожения химического оружия. Они характеризуются снижением выработки IgA до нижней границы нормы.
2. Изменения количества иммуноглобулинов класса IgА и специфических тиреоидных аутоантител (анти-ТГ IgG и анти-ТПО IgG) являются донозологическими проявлениями функциональных отклонений в иммунной системе с рисками развития в дальнейшем манифестации заболевания в виде аутоиммунного тиреоидита или диффузного нетиреоидного зоба.







